По мере роста глобального спроса на устойчивые и экономически эффективные решения для хранения энергии натрий-ионные (Na-ion) аккумуляторы становятся привлекательной альтернативой традиционным литий-ионным (Li-ion) технологиям. Благодаря обилию сырьевых материалов, меньшему воздействию на окружающую среду и перспективным электрохимическим характеристикам, натрий-ионные аккумуляторы быстро завоевывают популярность в различных областях — от крупномасштабного хранения энергии до электромобилей и потребительской электроники. В основе этой инновации лежит фундаментальный электрохимический процесс: обратимое перемещение ионов натрия между катодом и анодом во время зарядки и разрядки. В данной статье мы рассмотрим сложные механизмы, управляющие циклами заряда и разряда натрий-ионных аккумуляторов, раскрывая причины, по которым эта технология готова изменить будущее хранения энергии.
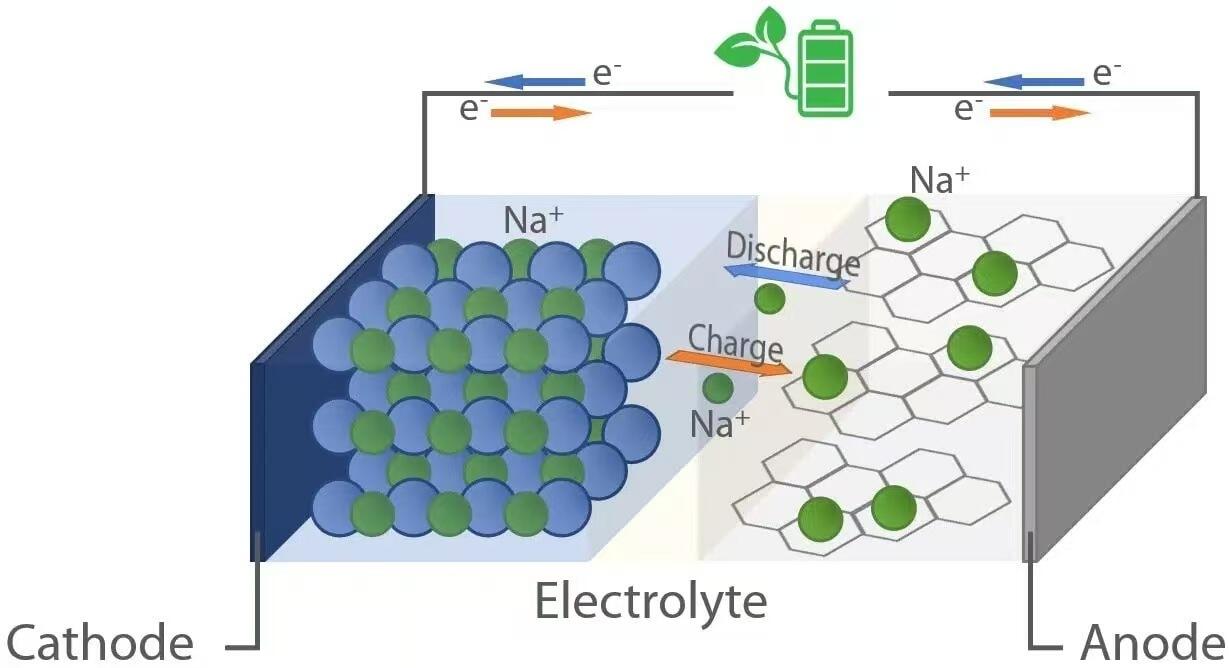
Как и их аналоги на основе литий-ионных технологий, натрий-ионные аккумуляторы работают по принципу «качельной» электрохимии. Во время разряда — когда батарея питает устройство — ионы натрия (Na⁺) перемещаются от анода (отрицательного электрода) через электролит к катоду (положительному электроду). Одновременно электроны проходят по внешней цепи, подавая электрическую энергию к подключённой нагрузке. Напротив, во время зарядки внешний источник питания возвращает ионы натрия из катода обратно к аноду, накапливая энергию для последующего использования. Этот обратимый процесс перемещения ионов обеспечивается материалами-носителями в обоих электродах, которые могут обратимо интеркалировать (вводить) и деинтеркалировать (извлекать) ионы натрия без значительного структурного разрушения.
При разрядке натрий-ионной батареи на аноде происходит окисление. Обычными материалами анода являются, например, твёрдый углерод, обладающий неупорядоченной структурой с нанопорами, способными вместить ионы Na⁺. По мере того как батарея отдаёт энергию, атомы натрия в аноде отдают электроны (e⁻) и превращаются в ионы Na⁺:
Анод (Окисление):
Na → Na⁺ + e⁻
Эти электроны проходят через внешнюю цепь, обеспечивая питание устройств, в то время как ионы Na⁺ перемещаются через жидкий или твёрдый электролит в сторону катода. На катоде — который обычно состоит из слоистых оксидов переходных металлов (например, NaₓMO₂, где M = Mn, Fe, Ni и др.), полианионных соединений или аналогов берлинской лазури — происходит восстановление, при котором ионы Na⁺ и поступающие электроны внедряются в кристаллическую решётку:
Катод (Восстановление):
Na⁺ + e⁻ + Host → Na–Host
Это включение стабилизирует структуру катода и замыкает электрохимическую цепь. Напряжение, генерируемое при разряде, зависит от разницы электрохимического потенциала между материалами анода и катода и обычно составляет от 2,5 до 3,7 вольт для коммерческих Na-ионных элементов.
Во время зарядки к элементу прикладывается внешнее напряжение, превышающее напряжение холостого хода элемента, что приводит к обратному течению электрохимических реакций. Ионы натрия извлекаются из катода путем окисления:
Катод (окисление):
Na–Host → Na⁺ + e⁻ + Host
Освободившиеся ионы Na⁺ проходят через электролит обратно к аноду, а электроны возвращаются через внешний источник питания. На аноде происходит восстановление, при котором ионы Na⁺ соединяются с электронами и снова внедряются в углеродную матрицу:
Анод (восстановление):
Na⁺ + e⁻ → Na (интеркалированный)
Этот процесс восстанавливает запасенную в аккумуляторе энергию, подготавливая его к следующему циклу разрядки. Эффективная передача заряда, минимальное количество побочных реакций и структурная стабильность электродных материалов имеют решающее значение для достижения длительного срока службы и высокой кулоновской эффективности — ключевых показателей коммерческой жизнеспособности.
Электролит — обычно соль натрия (например, NaClO₄ или NaPF₆), растворенная в органических карбонатных растворителях, — играет ключевую роль в обеспечении быстрого переноса ионов при сохранении электрохимической стабильности. В начальных циклах зарядки на поверхности анода образуется твердый электролитный интерфазный слой (SEI). Этот пассивирующий слой предотвращает дальнейшее разложение электролита, одновременно позволяя ионам Na⁺ проходить через него — тонкий баланс, необходимый для безопасности и долговечности.
Естественное изобилие натрия (в более чем 1000 раз превышающее содержание лития в земной коре) приводит к снижению стоимости материалов и уменьшению геополитических рисков снабжения. Кроме того, в натрий-ионных батареях в качестве токосъёмника анода может использоваться алюминий (в отличие от литий-ионных, где требуется медь), что дополнительно снижает стоимость и массу. Однако ионы натрия крупнее и тяжелее ионов лития, что приводит к несколько более низкой энергетической плотности и более медленной диффузии. Текущие исследования сосредоточены на разработке передовых архитектур электродов, наноструктурированных материалов и твердотельных электролитов для преодоления этих ограничений.
Механизмы заряда и разряда натрий-ионных аккумуляторов демонстрируют изящный синергетический эффект между материаловедением и электрохимией, закладывая прочный фундамент для энергохранилищ следующего поколения. В отличие от литий-ионных аналогов, использование обильного и недорогого натрия не только снижает риски в цепочках поставок, но и соответствует глобальным целям устойчивого развития. По мере того как исследователи продолжают совершенствовать составы электродов — повышая стабильность и плотность энергии, оптимизировать составы электролитов для увеличения срока службы и безопасности, а также развивать процессы крупномасштабного производства для снижения себестоимости, натрий-ионная технология последовательно преодолевает оставшиеся технические барьеры. Этот прогресс создаёт предпосылки для трансформационной роли Na-ion аккумуляторов в декарбонизации энергетических систем по всему миру — от систем хранения энергии масштаба сети, поддерживающих интеграцию возобновляемых источников энергии, до портативных источников питания и электромобилей с низкой скоростью. Используя простое, но мощное движение ионов натрия, мы не просто эффективно и недорого храним электричество — мы формируем более доступное, устойчивое и экологически чистое энергетическое будущее. Эта технология служит мостом между научно-техническими инновациями и практическим применением, предлагая реальный путь к сокращению выбросов углерода и созданию более экологичной глобальной энергетической экосистемы.
 Горячие новости
Горячие новости