U skladu s člankom 5. stavkom 1. točkom (b) Uredbe (EU) br. 1290/2013, u skladu s člankom 5. stavkom 1. točkom (b) Uredbe (EU) br. 1290/2013, u okviru programa "Ujedinjeni europski narodi" (EU) u okviru programa "Ujedinjeni europski narodi" (EU) br. S obilnim sirovinama, manjim utjecajem na okoliš i obećavajućim elektrohemijskim performansama, Na-ionske baterije brzo dobijaju privlačnost u aplikacijama koje se kreću od skladištenja energije u mrežnom opsegu do električnih vozila i potrošačke elektronike. Središte ove inovacije je temeljni elektrohemijski proces: reverzibilno kretanje natrijumovih iona između katode i anode tijekom punjenja i pražnjenja. U ovom članku istražujemo složene mehanizme koji upravljaju ciklusima punjenja i pražnjenja natrijum-jonskih baterija, bacajući svjetlo na to zašto je ova tehnologija spremna preoblikovati budućnost skladištenja energije.
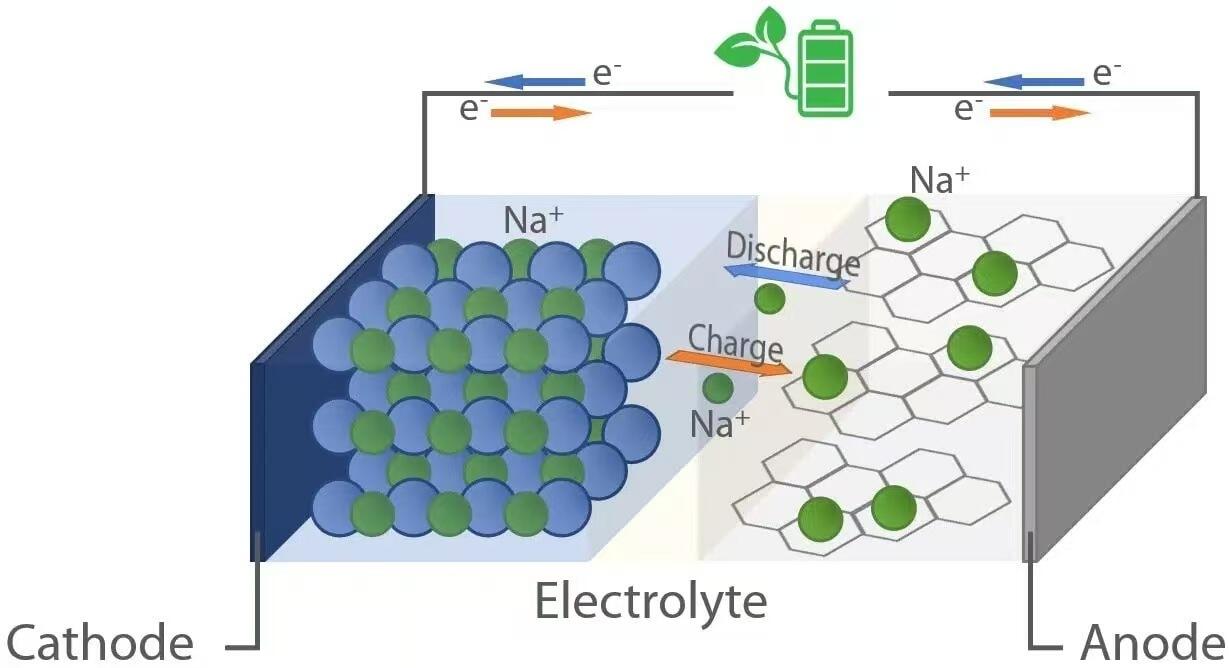
Kao i njihove litij-jonske kolege, natrijum-jonske baterije djeluju po principu elektrokemije stolice za ljuljanje. Tijekom pražnjenja, kada baterija napaja uređaj, ioni natrija (Na+) migriraju iz anode (negativne elektrode) kroz elektrolit do katode (pozitivne elektrode). Istovremeno, elektroni teče kroz vanjski krug, isporučujući električnu energiju povezanom opterećenju. Suprotno tome, tijekom punjenja, vanjski izvor napajanja vraća ione natrija iz katode u anodu, čuvajući energiju za buduću upotrebu. Ova reverzibilna ionska prebacivanja olakšava materijal domaćina u obje elektrode koji mogu reverzibilno interkalirati (umjestiti) i deinterkalirati (ekstraktirati) natrijeve ione bez značajne strukturne degradacije.
Kada se natrijum-jonska baterija isprazni, na anodi se javlja oksidacija. Uobičajeni anodni materijali uključuju tvrdi ugljik, koji ima poremećenu strukturu s nanoporima sposobnima za smještanje Na + iona. Kako baterija isporučuje snagu, atomi natrija unutar anode oslobađaju elektrone (e−) i postaju ioni Na+:
Sklopna površina:
Na → Na+ + e−
Ti elektroni putuju kroz vanjski krug do napajanja uređaja, dok se ioni Na + kreću kroz tekući ili čvrsti elektrolit prema katodi. Na katodi, koja se obično sastoji od slojevitih oksida prelaznih metala (npr. NaxMO2, gdje M = Mn, Fe, Ni, itd.), polianionskih spojeva ili analogi Pruske plave, dolazi do redukcije kako se ioni Na + i dolazni elektroni uključuju u kristalnu rešetku:
Katod (redukcija):
Na+ + e− + Domaćin → NaHost
Ova insertacija stabilizira strukturu katode i dovršava elektrohemijsko krug. Napon koji se stvara tijekom pražnjenja ovisi o razini elektrohemijskog potencijala između anodnog i katodnog materijala, obično u rasponu od 2,5 do 3,7 volti za komercijalne najonske ćelije.
Tijekom punjenja, primjenjuje se vanjski napon veći od napona otvorenog kružnog spoja ćelije, što unakrsno utječe na elektrohemijske reakcije. U slučaju da je to potrebno, u slučaju da je to potrebno, potrebno je upotrijebiti i druge metode.
Smanjenje i smanjenje emisije:
NaHost → Na+ + e− + Host
Oslobođeni Na+ ioni prolaze kroz elektrolit natrag do anode, dok se elektroni vraćaju putem vanjskog izvora energije. Na anodi, redukcija se događa kako se ioni Na+ kombinuju s elektronima i ponovno interkališu u ugljičnu matricu:
Smanjenje emisije:
Na+ + e− → Na (interkalirano)
Ovaj proces obnavlja pohranjenu energiju baterije, pripremajući je za sljedeći ciklus pražnjenja. Učinkovit prijenos naboja, minimalne sporedne reakcije i strukturna stabilnost materijala elektrode ključni su za postizanje dugog ciklusa života i visoke Kulombove učinkovitosti - ključnih mjera za komercijalnu održivost.
Elektrolit - obično natrijska sol (npr. NaClO4 ili NaPF6) rastvorena u organskim karbonatnim rastvaračima - igra ključnu ulogu u omogućavanju brzog transporta iona uz održavanje elektrohemijske stabilnosti. Tijekom početnih ciklusa punjenja, na površini anoda formira se interfaza čvrstog elektrolita (SEI). Ovaj sloj pasivacije sprječava daljnje razgradnje elektrolita, a omogućuje ioni Na+ da prođu kroz delikatnu ravnotežu koja je od suštinskog značaja za sigurnost i dugovječnost.
Prirodna obilnost natrija (više od 1000 puta češća od litijuma u Zemljinoj kori) rezultira nižim troškovima materijala i smanjenim geopolitičkim rizicima u opskrbi. Osim toga, aluminij se može koristiti kao prikupljač struje za anodu u Na-ionskim baterijama (za razliku od Li-ionskih, koje zahtijevaju bakar), što dodatno smanjuje troškove i težinu. Međutim, natrijum ioni su veći i teži od litijumskih iona, što rezultira nešto manjom gustinom energije i sporijom kinetikom difuzije. Trenutna istraživanja usmjerena su na razvoj naprednih arhitektura elektrode, nanostrukturiranih materijala i elektrolita u čvrstom stanju kako bi se nadvladali ovi ograničenja.
Mehanizmi punjenja i pražnjenja natrijum-jonskih baterija primjer su elegantne sinergije između znanosti o materijalima i elektrohemije, čime se postavlja čvrsta osnova za skladištenje energije sljedeće generacije. Za razliku od svojih litij-jonskih kolega, njihova ovisnost o obilnom, jeftinom natrijumu ne samo da ublažava rizike u lancu opskrbe, već se i usklađuje s globalnim ciljevima održivosti. Dok istraživači neprestano usavršavaju sastav elektroda povećavaju stabilnost i gustoću energije optimiziraju formulacije elektrolita kako bi povećali životni vijek i sigurnost ciklusa i unaprijedili velike proizvodne procese kako bi smanjili troškove proizvodnje, natrijev-jonska tehnologija postupno preva Iskoristivši jednostavno, ali moćno kretanje natrijevih iona, ne samo da smo efikasno i pristupačno skladištili struju, nego smo stvorili pristupačniju, otporniju i održiviju energiju u budućnosti. U skladu s člankom 21. stavkom 1.
 Najnovije vijesti
Najnovije vijesti