Naarmate de mondiale vraag naar duurzame en kostenefficiënte oplossingen voor energieopslag toeneemt, zijn natrium-ion (Na-ion) batterijen een aantrekkelijk alternatief geworden voor traditionele lithium-ion (Li-ion) technologieën. Met overvloedige grondstoffen, lagere milieubelasting en veelbelovende elektrochemische prestaties, winnen Na-ion batterijen snel aan belang in toepassingen die variëren van grootschalige opslag op het elektriciteitsnet tot elektrische voertuigen en consumentenelektronica. Aan de basis van deze innovatie ligt een fundamenteel elektrochemisch proces: de omkeerbare beweging van natriumionen tussen kathode en anode tijdens het opladen en ontladen. In dit artikel verkennen we de ingewikkelde mechanismen die de laad- en ontlaadcycli van natrium-ionbatterijen beheersen, en belichten we waarom deze technologie klaarstaat om de toekomst van energieopslag vorm te geven.
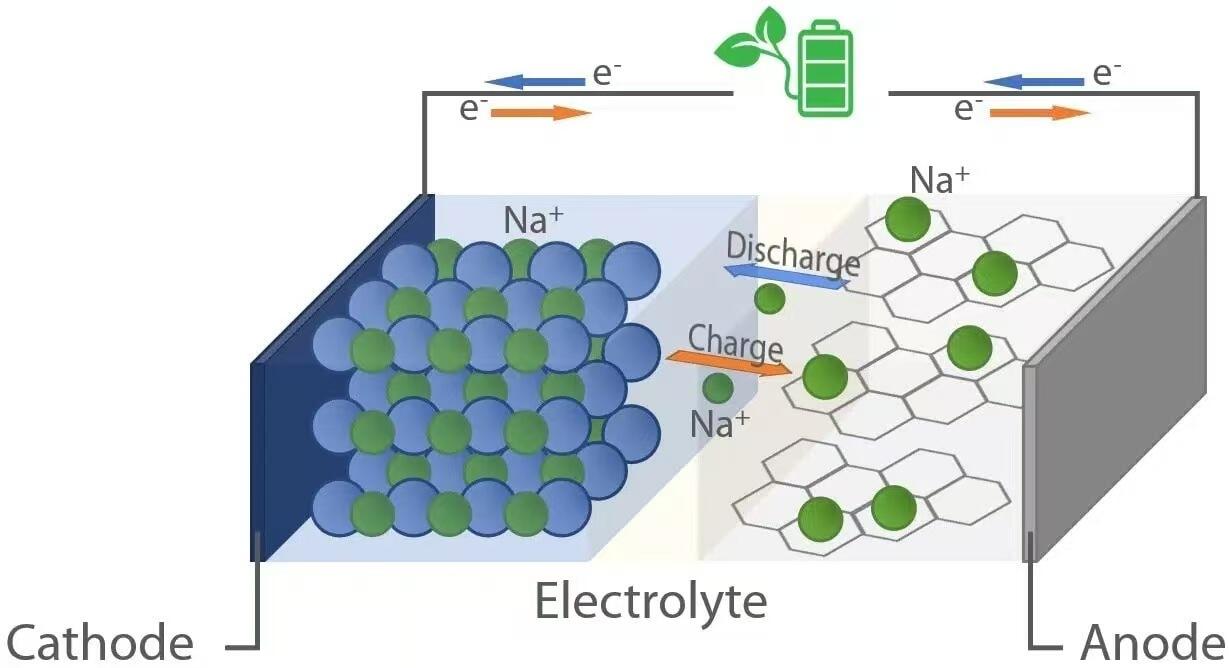
Net als hun lithium-ion tegenhangers werken natrium-ionbatterijen volgens het principe van de 'rocking-chair' electrochemie. Tijdens ontlading—wanneer de batterij een apparaat van stroom voorziet—verplaatsen natriumionen (Na⁺) zich van de anode (negatieve elektrode) via de elektrolyt naar de kathode (positieve elektrode). Tegelijkertijd stromen elektronen door de externe stroomkring en leveren elektrische energie aan de aangesloten belasting. Omgekeerd, tijdens het opladen, drijft een externe stroombron de natriumionen terug van de kathode naar de anode, waardoor energie wordt opgeslagen voor toekomstig gebruik. Deze omkeerbare ionentransport wordt vergemakkelijkt door gastmaterialen in beide elektroden die natriumionen kunnen reversibel intercaleren (invoegen) en desintercaleren (verwijderen) zonder significante structurele degradatie.
Wanneer een natrium-ionbatterij ontladen wordt, vindt oxidatie plaats aan de anode. Veelvoorkomende anodematerialen zijn onder andere hard koolstof, dat een geordende structuur met nanoporiën heeft die Na⁺-ionen kunnen opnemen. Terwijl de batterij stroom levert, geven natriumatomen in de anode elektronen (e⁻) af en worden Na⁺-ionen:
Anode (Oxidatie):
Na → Na⁺ + e⁻
Deze elektronen bewegen via de externe stroomkring om apparaten van stroom te voorzien, terwijl de Na⁺-ionen door de vloeibare of vaste elektrolyt naar de kathode migreren. Aan de kathode—meestal samengesteld uit gelaagde overgangsmetaaloxiden (bijv. NaₓMO₂, waarbij M = Mn, Fe, Ni, enz.), polyanionische verbindingen of analogen van Berlijns blauw—vindt reductie plaats wanneer Na⁺-ionen en binnenkomende elektronen in het kristalrooster worden opgenomen:
Kathode (Reductie):
Na⁺ + e⁻ + Host → Na–Host
Deze intercalatie stabiliseert de kathodestructuur en completeert de elektrochemische stroomkring. De tijdens ontlading gegenereerde spanning hangt af van het verschil in elektrochemisch potentiaal tussen de anode- en kathodematerialen, en ligt meestal tussen 2,5 en 3,7 volt voor commerciële Na-ion cellen.
Tijdens het laden wordt een externe spanning aangelegd die groter is dan de lege-celspanning van de cel, waardoor de elektrochemische reacties worden omgekeerd. Natriumionen worden uit de kathode geëxtraheerd via oxidatie:
Kathode (Oxidatie):
Na–Host → Na⁺ + e⁻ + Host
De vrijgekomen Na⁺-ionen bewegen door de elektrolyt terug naar de anode, terwijl de elektronen via de externe stroombron retourkeren. Aan de anode vindt reductie plaats wanneer Na⁺-ionen zich met elektronen verenigen en opnieuw in de koolstofmatrix worden geïntercaleerd:
Anode (Reductie):
Na⁺ + e⁻ → Na (geïntercaleerd)
Dit proces herstelt de opgeslagen energie van de batterij, waardoor deze klaar is voor de volgende ontladingscyclus. Efficiënte ladingsoverdracht, minimale nevenreacties en structurele stabiliteit van elektrodematerialen zijn cruciaal om een lange levensduur en hoge Coulomb-efficiëntie te bereiken — belangrijke parameters voor commerciële haalbaarheid.
De elektrolyt — meestal een natriumzout (bijvoorbeeld NaClO₄ of NaPF₆) opgelost in organische carbonaatsolventen — speelt een centrale rol bij het mogelijk maken van snelle ionentransport terwijl elektrochemische stabiliteit behouden blijft. Tijdens de eerste laadcycli vormt zich een vaste elektrolytinterfase (SEI) op het anodeoppervlak. Deze passiverende laag voorkomt verdere ontleding van de elektrolyt, terwijl deze wel Na⁺-ionen doorlaat — een fijn evenwicht dat essentieel is voor veiligheid en levensduur.
De natuurlijke overvloed van natrium (meer dan 1.000 keer vaker aanwezig dan lithium in de aardkorst) zorgt voor lagere materiaalkosten en verminderde geopolitieke leveringsrisico's. Daarnaast kan aluminium worden gebruikt als stroomafnemer voor de anode in Na-ionbatterijen (in tegenstelling tot Li-ion, dat koper vereist), wat de kosten en het gewicht verder verlaagt. Natriumionen zijn echter groter en zwaarder dan lithiumionen, wat leidt tot een iets lagere energiedichtheid en langzamere diffusiekinetiek. Lopend onderzoek richt zich op de ontwikkeling van geavanceerde elektrode-architecturen, nano-gestructureerde materialen en vaste elektrolyten om deze beperkingen te overwinnen.
De laad- en ontlaadmechanismen van natrium-ionbatterijen zijn een voorbeeld van de elegante synergie tussen materiaalkunde en elektrochemie, en leggen een solide basis voor opslag van energie van de volgende generatie. In tegenstelling tot lithium-ionbatterijen verkleint het gebruik van overvloedig en goedkoop natrium niet alleen de risico's in de aanvoerketen, maar sluit het ook aan bij de mondiale duurzaamheidsdoelstellingen. Naarmate onderzoekers continu de samenstelling van elektroden verbeteren — met name stabiliteit en energiedichtheid — elektrolytformuleringen optimaliseren om de levensduur en veiligheid te verhogen, en grootschalige productieprocessen verder ontwikkelen om productiekosten te verlagen, overwint de natrium-iontechnologie geleidelijk de resterende technische belemmeringen. Deze vooruitgang zorgt ervoor dat natrium-ionbatterijen een transformatieve rol kunnen spelen in de decarbonisatie van energiesystemen wereldwijd, van op grote schaal opgeslagen energie ter ondersteuning van integratie van hernieuwbare energiebronnen tot draagbare stroomvoorziening en elektrische mobiliteit met lage snelheid. Door gebruik te maken van de eenvoudige maar krachtige beweging van natriumionen slaan we niet alleen efficiënt en betaalbaar elektriciteit op — we vormen ook een toegankelijkere, veerdere en duurzamere energietoekomst. Het sluit de kloof tussen technologische innovatie en praktische toepassing, en biedt een haalbare weg om koolstofemissies te verminderen en een groener mondiaal energiesysteem op te bouwen.