Eftersom den globale efterspørgsel efter bæredygtige og omkostningseffektive energilagringsløsninger tiltager, er natrium-ion (Na-ion) batterier fremtrådt som et attraktivt alternativ til de traditionelle lithium-ion (Li-ion) teknologier. Med rigelige råmaterialer, lavere miljøpåvirkning og lovende elektrokemiske ydeevne vinder Na-ion batterier hurtigt indpasning i anvendelser fra netstørrelse energilagring til elbiler og forbruger elektronik. I centrum for denne innovation ligger en grundlæggende elektrokemisk proces: den reversible bevægelse af natriumioner mellem katode og anode under opladning og afladning. I denne artikel udforsker vi de komplekse mekanismer, der styrer opladnings- og afladningscyklusserne i natrium-ion batterier, og belyser, hvorfor denne teknologi er på vej til at omforme fremtidens energilagring.
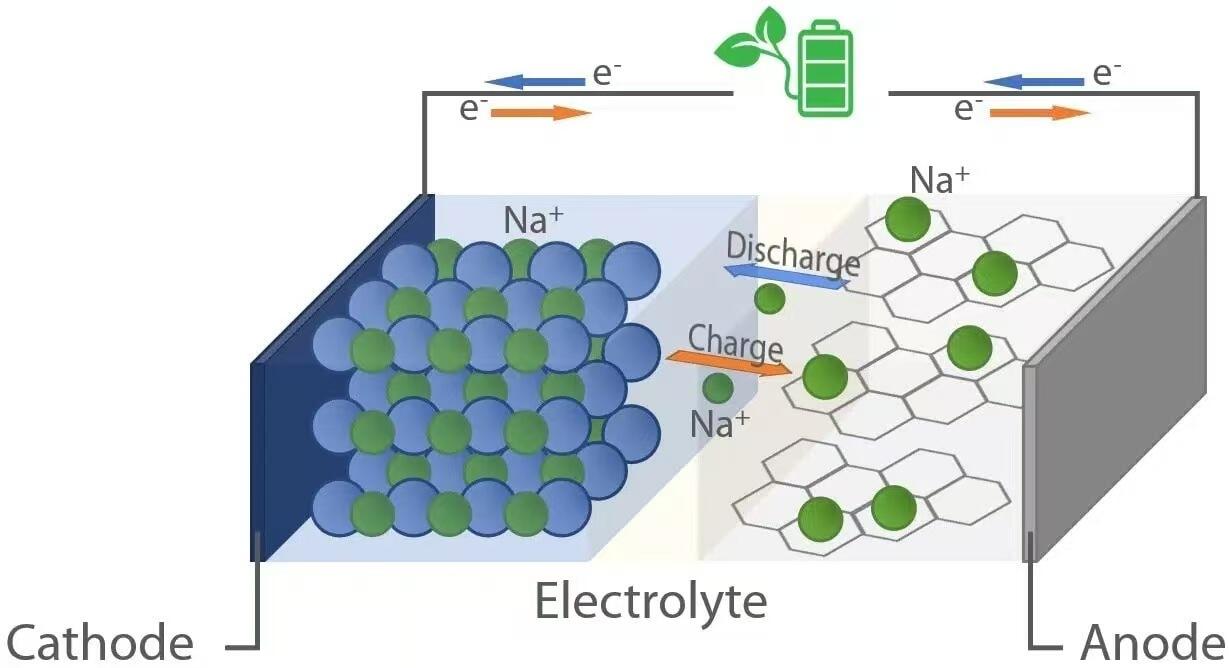
Ligesom deres litiumpartnerskaber fungerer natrium-ionbatterier efter princippet om "rocking-chair"-elektrokemi. Under afladning – når batteriet forsyner en enhed med strøm – vandrer natriumioner (Na⁺) fra anoden (negativ elektrode) gennem elektrolytten til katoden (positiv elektrode). Samtidig strømmer elektronerne gennem den eksterne kreds, hvilket leverer elektrisk energi til den tilsluttede belastning. Omvendt, under opladning, presser en ekstern strømkilde natriumionerne tilbage fra katoden til anoden og lagrer derved energi til senere brug. Dette reversible iontransport er muliggjort af værtsmaterialer i begge elektroder, som kan reversibelt interkalere (indsætte) og deinterkalere (fjerne) natriumioner uden væsentlig strukturel nedbrydning.
Når en natrium-ionebatteri aflades, sker oxidation ved anoden. Almindelige anodematerialer inkluderer hærdet kulstof, som har en uordnet struktur med nanoporer, der kan rumme Na⁺-ioner. Når batteriet leverer strøm, afgiver natriumatomer i anoden elektroner (e⁻) og bliver til Na⁺-ioner:
Anode (Oxidation):
Na → Na⁺ + e⁻
Disse elektroner vandrer gennem den eksterne kreds for at drive elektriske enheder, mens Na⁺-ionerne bevæger sig gennem den flydende eller faste elektrolyt mod katoden. Ved katoden – typisk sammensat af lagdelte overgangsmetaloxider (f.eks. NaₓMO₂, hvor M = Mn, Fe, Ni osv.), polyanioniske forbindelser eller Prussian blue-analoger – sker reduktion, når Na⁺-ioner og indkomne elektroner integreres i krystalgitteret:
Katode (Reduktion):
Na⁺ + e⁻ + Vært → Na–Vært
Denne indsættelse stabiliserer katodestrukturen og afslutter den elektrokemiske kreds. Den spænding, der genereres under afladning, afhænger af forskellen i elektrokemisk potentiale mellem anode- og katodematerialer, typisk i området 2,5 til 3,7 volt for kommercielle Na-ion celler.
Under opladning påføres en ekstern spænding, som er højere end cellens åbne kredsløbsspænding, hvilket vender de elektrokemiske reaktioner om. Natriumioner udvindes fra katoden gennem oxidation:
Katode (oxidation):
Na–Vært → Na⁺ + e⁻ + Vært
De frigivne Na⁺ ioner vandrer gennem elektrolytten tilbage til anoden, mens elektronerne vender tilbage via den eksterne strømkilde. Ved anoden sker reduktion, når Na⁺ ioner kombineres med elektroner og genindlejres i kulstofmatricen:
Anode (reduktion):
Na⁺ + e⁻ → Na (indlejret)
Denne proces genopretter batteriets lagrede energi og forbereder det til den næste afladningscyklus. Effektiv opladningsoverførsel, minimale bivirkninger og strukturel stabilitet af elektrodematerialer er afgørende for at opnå lang cykluslevetid og høj coulombisk efficiens – nøgletal for kommerciel levedygtighed.
Elektrolytten – typisk et natriumsalt (f.eks. NaClO₄ eller NaPF₆) opløst i organiske carbonatopløsningsmidler – spiller en afgørende rolle for muliggørelse af hurtig ionetransport samtidig med opretholdelse af elektrokemisk stabilitet. I de første opladningscykluser dannes der en fast elektrolytgrænseflade (SEI) på anodens overflade. Dette passiveringslag forhindrer yderligere nedbrydning af elektrolytten, mens det tillader Na⁺-ioner at passere igennem – en følsom balance, som er afgørende for sikkerhed og levetid.
Natrums naturlige forekomst (mere end 1.000 gange mere udbredt end lithium i jordskorpen) resulterer i lavere materialeomkostninger og reducerede geopolitiske forsyningsrisici. Desuden kan aluminium anvendes som strømsamler til anoden i Na-ion-batterier (i modsætning til Li-ion, som kræver kobber), hvilket yderligere formindsker omkostninger og vægt. Dog er natriumioner større og tungere end lithiumioner, hvilket resulterer i en let lavere energitæthed og langsommere diffusionskinetik. Ongoing forskning fokuserer på at udvikle avancerede elektrodearkitekturer, nanostrukturerede materialer og faste elektrolytter for at overvinde disse begrænsninger.
Opladnings- og afladningsmekanismerne i natrium-ionbatterier er et eksempel på den elegante sammenhæng mellem materialevidenskab og elektrokemi, hvilket skaber et solidt grundlag for energilagring af næste generation. I modsætning til litium-ion-batterier reducerer deres brug af det rigelige og billige natrium ikke kun risici i forsyningskæden, men støtter også globale bæredygtighedsmål. Mens forskere løbende forbedrer elektrodekompositioner – for at øge stabilitet og energitæthed – optimerer elektrolytformuleringer for at forlænge cykluslevetid og sikkerhed samt udvikler produktionsprocesser i stor målestok for at sænke produktionsomkostninger, overvinder natrium-ion-teknologien gradvist de sidste tekniske barrierer. Denne udvikling stiller Na-ion-batterier i en position til at spille en transformerende rolle i decarboniseringen af energisystemer verden over, fra netstørrelse lagring, der understøtter integration af vedvarende energi, til bærbar strøm og lavhastigheds elektrisk mobilitet. Ved at udnytte den simple, men kraftfulde bevægelse af natriumioner lagrer vi ikke blot elektricitet effektivt og økonomisk – vi skaber en mere tilgængelig, robust og bæredygtig energifremtid. Det udbridger kløften mellem teknologisk innovation og praktisk anvendelse og tilbyder en realistisk vej til at reducere CO2-udledning og opbygge et grønnere globalt energisystem.
 Seneste nyheder
Seneste nyheder