Seiring meningkatnya permintaan global terhadap solusi penyimpanan energi yang berkelanjutan dan hemat biaya, baterai natrium-ion (Na-ion) telah muncul sebagai alternatif menarik dibanding teknologi lithium-ion (Li-ion) tradisional. Dengan bahan baku yang melimpah, dampak lingkungan yang lebih rendah, serta kinerja elektrokimia yang menjanjikan, baterai Na-ion semakin mendapatkan perhatian dalam berbagai aplikasi, mulai dari penyimpanan energi skala jaringan hingga kendaraan listrik dan perangkat elektronik konsumen. Di inti inovasi ini terdapat proses elektrokimia mendasar: pergerakan bolak-balik ion natrium antara katoda dan anoda selama pengisian dan pelepasan muatan. Dalam artikel ini, kami mengulas mekanisme rumit yang mengatur siklus pengisian dan pelepasan muatan pada baterai natrium-ion, memberikan wawasan mengapa teknologi ini siap membentuk masa depan penyimpanan energi.
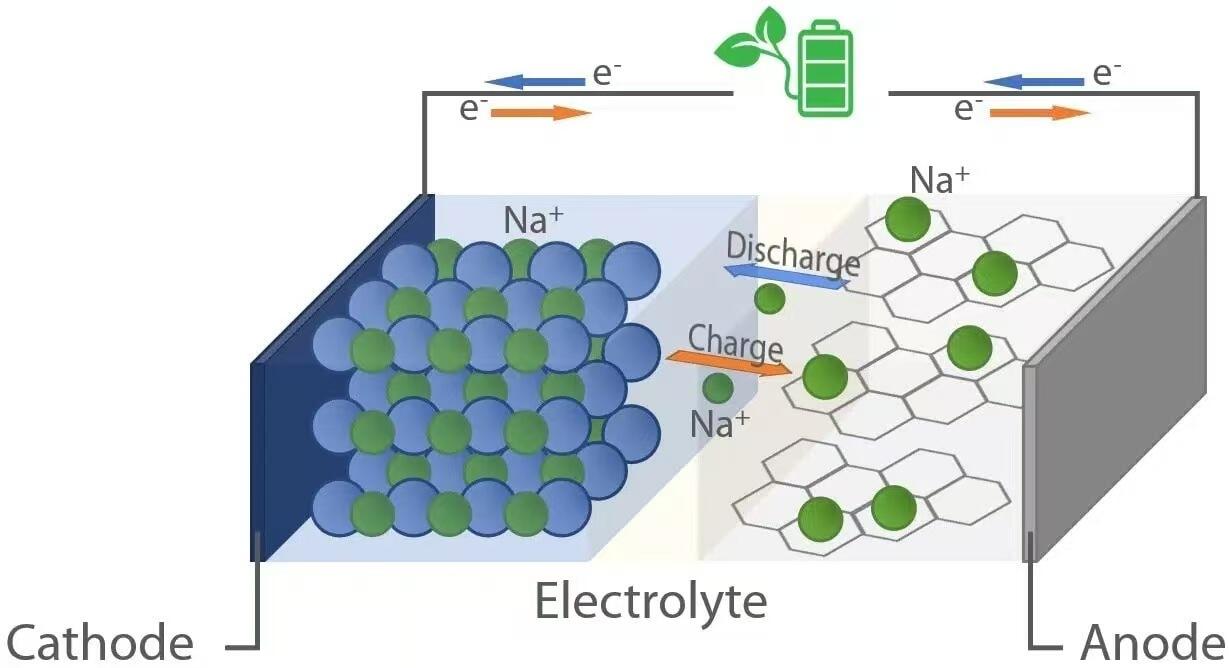
Sama seperti baterai lithium-ion, baterai sodium-ion beroperasi berdasarkan prinsip elektrokimia "rocking-chair". Selama proses pelepasan muatan—ketika baterai menghidupkan perangkat—ion natrium (Na⁺) berpindah dari anoda (elektroda negatif) melalui elektrolit menuju katoda (elektroda positif). Secara bersamaan, elektron mengalir melalui rangkaian eksternal, mengirimkan energi listrik ke beban yang terhubung. Sebaliknya, selama pengisian, sumber daya eksternal mendorong ion natrium kembali dari katoda ke anoda, menyimpan energi untuk digunakan di kemudian hari. Perpindahan ion yang dapat dibalik ini difasilitasi oleh material pembawa pada kedua elektroda yang mampu menginterkalasi (memasukkan) dan mendekinterkalasi (mengeluarkan) ion natrium secara reversibel tanpa mengalami degradasi struktural yang signifikan.
Ketika baterai natrium-ion melakukan pengosongan, oksidasi terjadi di anoda. Bahan anoda yang umum termasuk karbon keras, yang memiliki struktur tidak teratur dengan nanopori yang mampu menampung ion Na⁺. Saat baterai mengeluarkan daya, atom natrium di dalam anoda melepaskan elektron (e⁻) dan berubah menjadi ion Na⁺:
Anoda (Oksidasi):
Na → Na⁺ + e⁻
Elektron-elektron ini bergerak melalui rangkaian eksternal untuk memberi daya pada perangkat, sementara ion Na⁺ bergerak melalui elektrolit cair atau padat menuju katoda. Di katoda—yang biasanya terdiri dari oksida logam transisi berlapis (misalnya NaₓMO₂, dengan M = Mn, Fe, Ni, dll.), senyawa polianionik, atau analog Prussian blue—reduksi terjadi saat ion Na⁺ dan elektron masuk terintegrasi ke dalam kisi kristal:
Katoda (Reduksi):
Na⁺ + e⁻ + Host → Na–Host
Insersi ini menstabilkan struktur katoda dan melengkapi rangkaian elektrokimia. Tegangan yang dihasilkan selama pelepasan muatan bergantung pada perbedaan potensial elektrokimia antara bahan anoda dan katoda, yang biasanya berkisar antara 2,5 hingga 3,7 volt untuk sel Na-ion komersial.
Selama pengisian, tegangan eksternal yang lebih besar dari tegangan sirkuit terbuka sel diterapkan, membalikkan reaksi elektrokimia. Ion natrium diekstraksi dari katoda melalui oksidasi:
Katoda (Oksidasi):
Na–Host → Na⁺ + e⁻ + Host
Ion Na⁺ yang dilepaskan melintasi elektrolit kembali ke anoda, sementara elektron kembali melalui sumber daya eksternal. Di anoda, reduksi terjadi saat ion Na⁺ bergabung dengan elektron dan kembali menginterkalasi ke dalam matriks karbon:
Anoda (Reduksi):
Na⁺ + e⁻ → Na (terinterkalasi)
Proses ini mengembalikan energi yang tersimpan dalam baterai, mempersiapkannya untuk siklus pelepasan berikutnya. Transfer muatan yang efisien, reaksi samping minimal, dan stabilitas struktural material elektroda sangat penting untuk mencapai umur siklus yang panjang dan efisiensi Coulombic yang tinggi—parameter kunci untuk kelayakan komersial.
Elektrolit—biasanya garam natrium (misalnya NaClO₄ atau NaPF₆) yang dilarutkan dalam pelarut karbonat organik—memainkan peran penting dalam memungkinkan transportasi ion yang cepat sekaligus menjaga stabilitas elektrokimia. Selama siklus pengisian awal, terbentuk lapisan antarmuka padat-elektrolit (SEI) pada permukaan anoda. Lapisan pasif ini mencegah dekomposisi elektrolit lebih lanjut sambil tetap memungkinkan ion Na⁺ melewatinya—keseimbangan halus yang esensial bagi keselamatan dan umur panjang baterai.
Kelimpahan alam natrium (lebih dari 1.000 kali lebih banyak daripada litium di kerak bumi) menyebabkan biaya material yang lebih rendah dan mengurangi risiko pasokan geopolitik. Selain itu, aluminium dapat digunakan sebagai kolektor arus untuk anoda dalam baterai Na-ion (tidak seperti Li-ion yang memerlukan tembaga), sehingga semakin menekan biaya dan bobot. Namun, ion natrium lebih besar dan lebih berat dibandingkan ion litium, menghasilkan kepadatan energi yang sedikit lebih rendah serta kinetika difusi yang lebih lambat. Penelitian yang sedang berlangsung berfokus pada pengembangan arsitektur elektroda canggih, material nanostruktur, dan elektrolit padat untuk mengatasi keterbatasan ini.
Mekanisme pengisian dan pelepasan baterai ion natrium menunjukkan sinergi elegan antara ilmu material dan elektrokimia, yang meletakkan fondasi kuat bagi penyimpanan energi generasi berikutnya. Berbeda dengan baterai ion lithium, ketergantungan pada natrium yang melimpah dan berbiaya rendah tidak hanya mengurangi risiko dalam rantai pasok, tetapi juga selaras dengan tujuan keberlanjutan global. Seiring peneliti terus menyempurnakan komposisi elektroda—meningkatkan stabilitas dan kepadatan energi—mengoptimalkan formulasi elektrolit untuk memperpanjang masa siklus dan keselamatan, serta memajukan proses manufaktur skala besar demi menekan biaya produksi, teknologi ion natrium secara mantap mengatasi hambatan teknis yang tersisa. Kemajuan ini menempatkan baterai Na-ion untuk memainkan peran transformatif dalam mendekarbonisasi sistem energi di seluruh dunia, dari penyimpanan skala jaringan yang mendukung integrasi energi terbarukan hingga tenaga portabel dan mobilitas listrik berkecepatan rendah. Dengan memanfaatkan gerakan ion natrium yang sederhana namun kuat, kita tidak hanya menyimpan listrik secara efisien dan terjangkau—kita sedang menciptakan masa depan energi yang lebih mudah diakses, tangguh, dan berkelanjutan. Ini menjembatani kesenjangan antara inovasi teknologi dan aplikasi dunia nyata, menawarkan jalur yang layak untuk mengurangi emisi karbon dan membangun ekosistem energi global yang lebih hijau.